先ほどの実験を化学反応式で表すと 2Cu + O 2 → 2CuO と表すことができます。 これは、銅が酸化されて、酸化銅(II)になったということです。試験によく出る! 化学反応式一覧鉄と硫黄の化合 Fe+S→FeS (鉄+硫黄→硫化鉄)銅と酸素の化合 2Cu+O2→2CuO (銅+酸素→酸化銅)化学の問題です。酸化銅(II)CuOを炭素Cによって還元すると、銅と二酸化炭素が生じる。酸化銅(II)24gを炭素と反応さすた。下の化学反応式を使って下さい。2CuO C→2Cu CO2⑴酸化銅(Ⅱ)と反応する炭素はmolか。CuO 2molとC 1molの反
中2理科 酸化銅の還元 酸化も同時に起こる反応 Pikuu
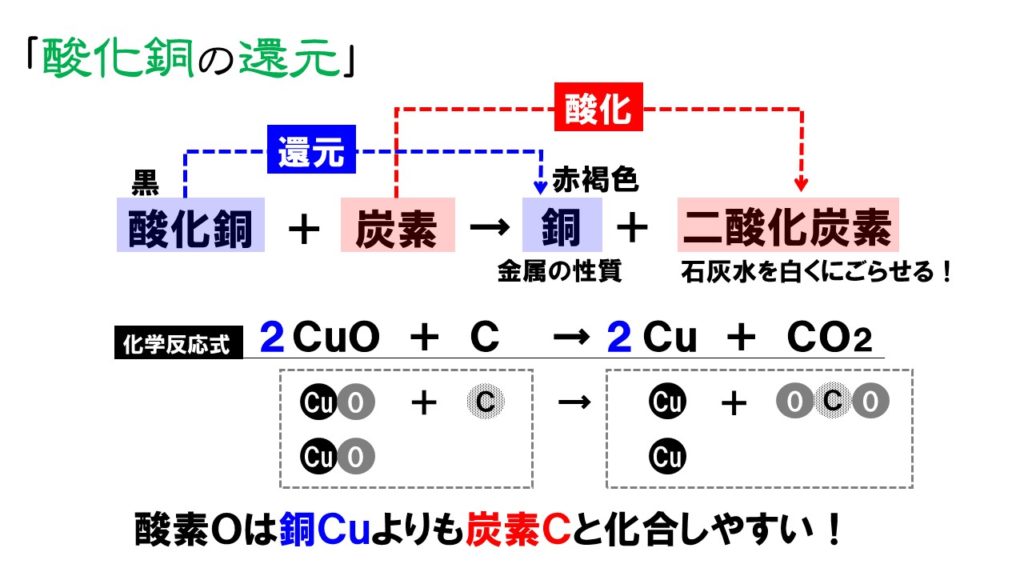
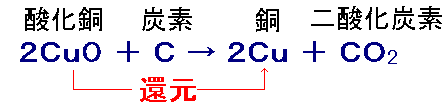
酸化銅 炭素→銅 二酸化炭素化学反応式
酸化銅 炭素→銅 二酸化炭素化学反応式-酸化銅と炭素の混合物を熱する 2CuO C → 2Cu CO 2 酸化銅の酸素が炭素と反応して二酸化炭素になることで、銅が還元される。 酸化鉄に水素を送りながら熱する Fe 3 O 4 4H 2 → 3Fe 4H 2 O 酸化鉄の酸素が水素と反応して水になることで、鉄が還元される。銅+酸素→酸化銅 2Cu O₂ → 2CuO



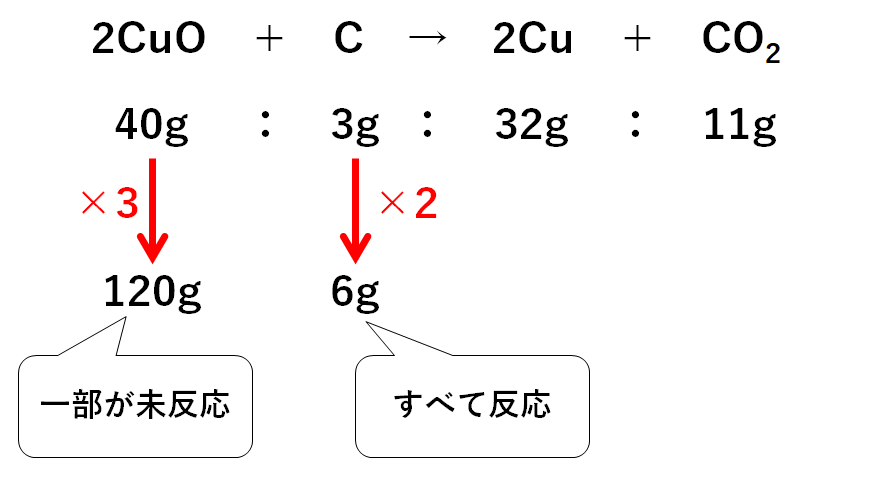
化学変化の計算問題
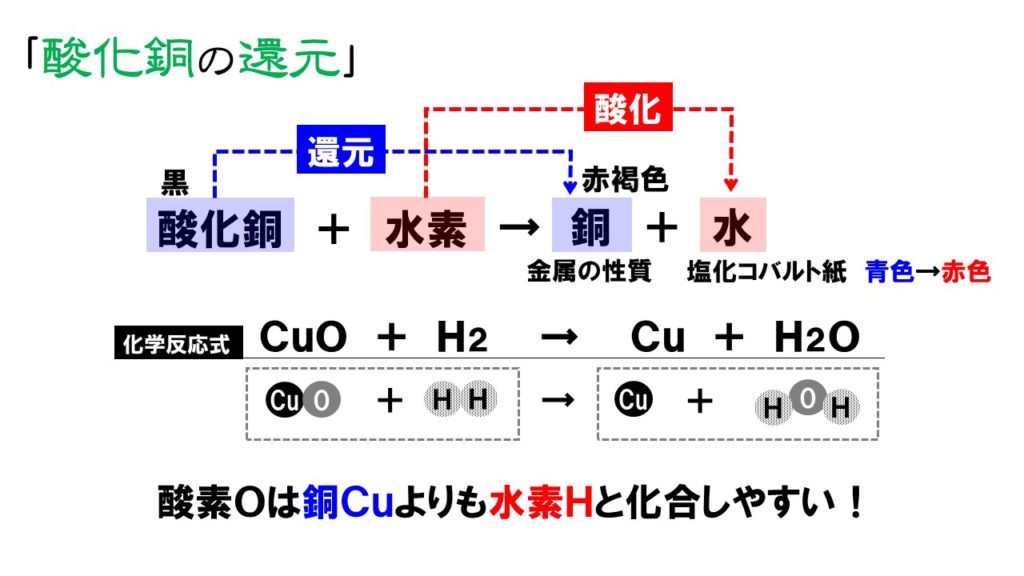
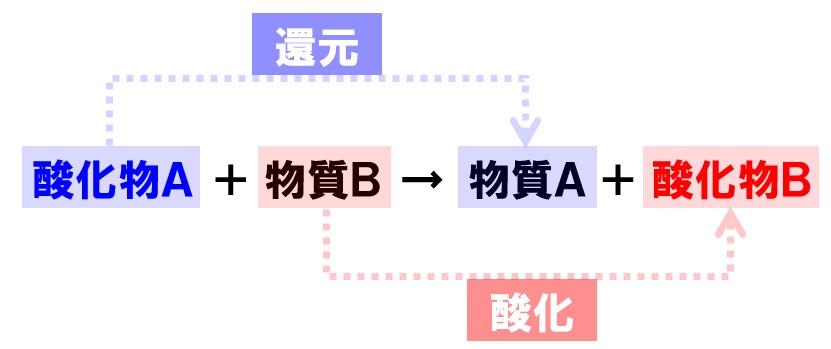
この時の化学反応式は「Cu(OH)2 → CuO H2O」となります。る。炭素の酸化の反応速度論や炭素表面の酸素の吸脱着現象 に関する解説は,過去の実験技術講座1)や新・炭素材料入門2) に優れた解説があるので省略させていただく。 一般に,化学反応式に従った反応が起こるか否かは,反応前酸化物が 二酸化炭素 <まとめ> 1 酸化銅に炭素を混ぜて熱すると,銅と( )ができる。この化学変化 を,化学反応式で表すと,次のようになる。 ( )+( ) ( )+( ) 2 熱した酸化銅を水素に入れると,銅と( )ができる。この化学変化を,
化学反応式を記号として覚えようとしても難しいと思います。 2つの要点を抑えて覚えていけると良いと思います。 ただ、反応自体も覚えておいてください。 例えば「過酸化水素水と二酸化マンガンで水と酸素ができる」みたいな事は、反応性の乏しい物質である。この二酸化炭素を炭素源として触媒的に有用物質の合 成に利用することが出来れば,次世代炭素源の開発という見地からも重要であろう1。 二酸化炭素の反応は,(1) 水素–炭素結合生成反応, (2) 酸素–炭素結合生成反応,化学反応式 化学変化3 酸化銀を熱分解すると,銀と酸素ができる。 化学反応式 化学変化4 鉄と硫黄の混合物を加熱すると,硫化鉄がで きる。 化学反応式 化学変化5 酸化銅と炭を混ぜて加熱すると,二酸化炭素 が発生し,金属の銅ができる。 化学反応式
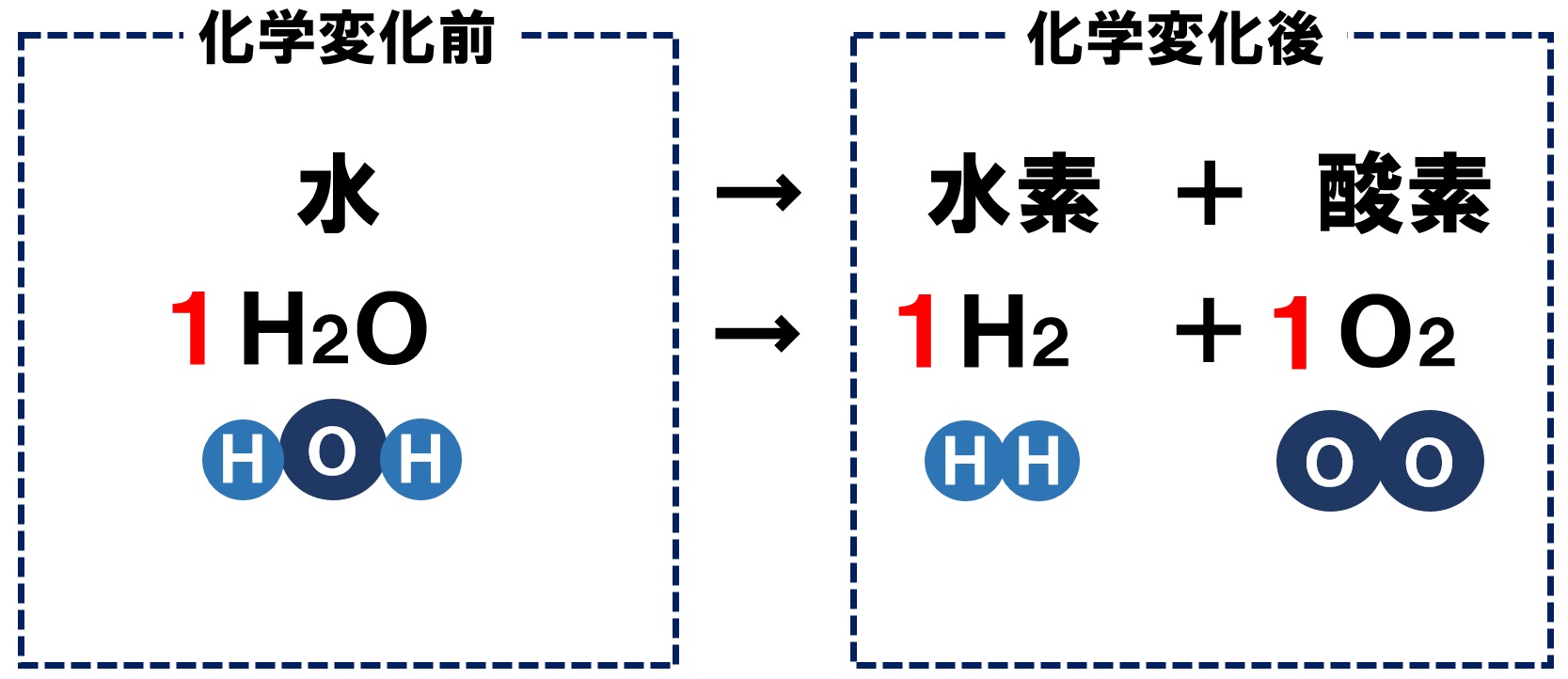
5 覚えておきたい8つの重要な化学反応式 51 1鉄と硫黄を加熱すると硫化鉄ができる 52 2炭素を燃焼すると二酸化炭素ができる 521 化学式を諳記しなければ、化学反応式は作れない! 53 3水を電気分解すると水素と酸素ができる 531 原子が一致しない二酸化炭素 ( CO 2) の再資源化に向けた触媒技術 化学反応が進む際の反応速度は,一般に反応が進む際の が生成される.一方で,Ni の代わりに銅 ( Cu ) と酸化銅の還元の中学生向け解説ページ です。 「 酸化銅の還元 」 は中学2年生の化学で学習します。 還元とは何か 酸化銅の還元 の実験動画 酸化銅の還元の化学反応式(炭素)



中学理科酸化銅の還元の問題です 酸化銅4gと炭素の粉末を混 Yahoo 知恵袋



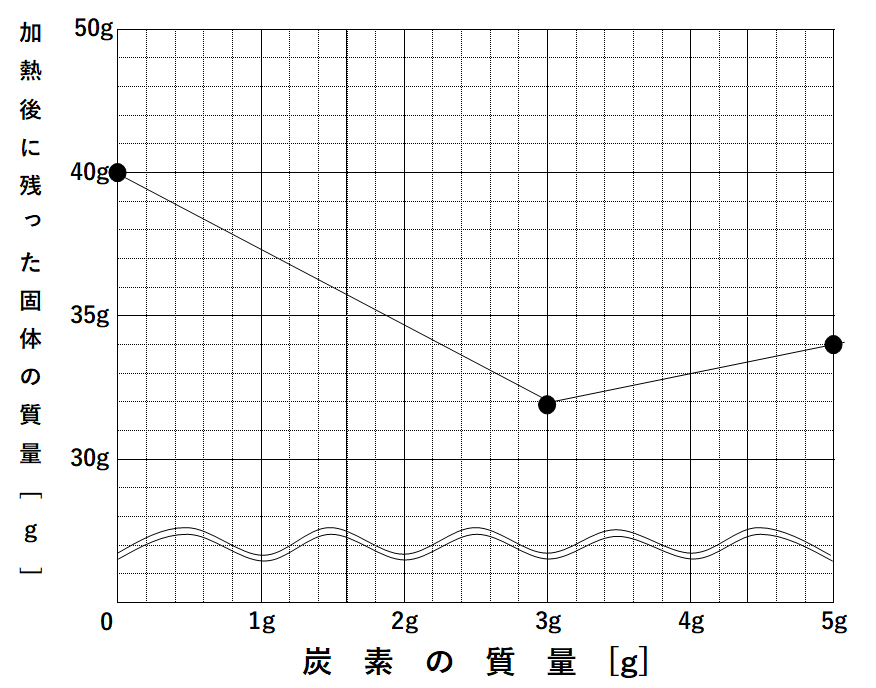
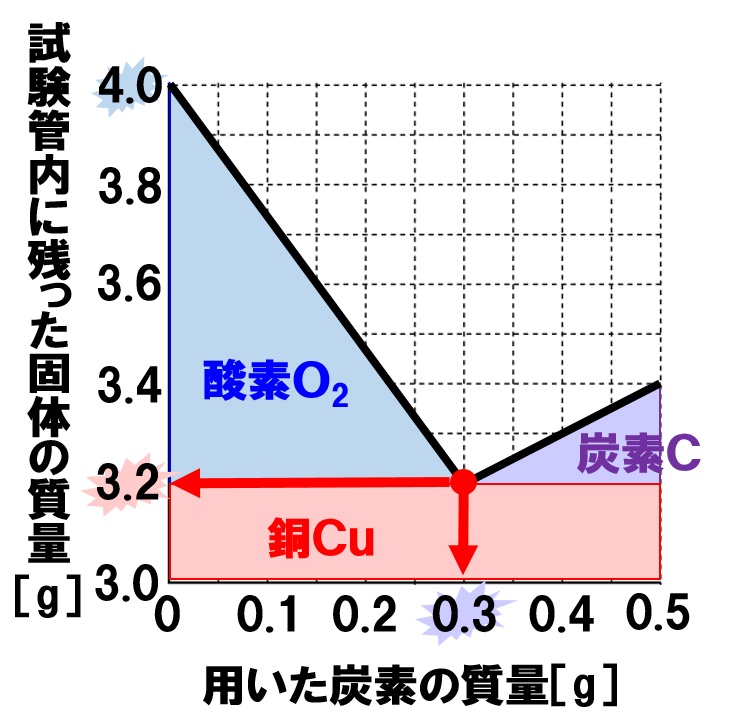
酸化銅の還元の実験で グラフがこのような形になる理由を教えてください Yahoo 知恵袋
二酸化塩素が化学物質として認識されたのは19世紀 の初めのことであるが,1921年にSchmidtとGrau・ mannが初めて二酸化塩素で木片を処理しホロセルロ ースを調製した。これは二酸化塩素が適当な条件下では セルロースをいためない特性によるもので,セル誉一ス水や二酸化炭素など、化学式が2種類以上の原子記号をふくんでいるものは化合物である。 化合物水H2O 二酸化炭素CO2 塩化ナトリウムNaCl 酸化銅CuO 酸化マグネシウムMgO 塩酸(塩化水素)HCl 水酸化ナトリウムNaOH アンモニアNH3銅を熱すると酸素と結びつきます。 銅 + 酸素 → 酸化銅 (※ 虹色の銅) 炭素を熱しても酸素と結びつきます。 炭素 + 酸素 → 二酸化炭素 ( →鉄が燃えると二酸化炭素は出ない? もし銅と炭素を同時に熱すると、当然ですが、酸化銅と二酸化炭素ができます。



Http Www Subaru Net Com Wp Content Uploads 18 03 18rika Mondai Pdf




Pi Descubre Como Resolverlo En Qanda
る。銅が空気中の水分と二酸化炭素の作用で反応すると,塩基性炭酸銅 CuCO 3 ・ Cu (OH) 2 になる。空気中に二酸化硫黄または硫化水素が微量存在すると, これと反応し,さらに酸化されて CuSO 4 ・ 3 Cu (OH) 2 が生じる。酸化銅炭素→二酸化炭素銅 となりますね。 さらに、化学式で表してみましょう。 酸化銅は銅に酸素がくっついたCuOという式で表されます。また、炭素はCです。 出来上がる物質として二酸化炭素がありますが、これはCO 2 と表されます。また、銅はCuとFdData中間期末:中学理科2年化学 さまざまな化学反応式 パソコン・タブレット版へ移動 炭素と酸素の化合 問題(1学期中間) 次の図は木炭(炭素 )が酸素と化合して 二酸化炭素ができる反応を表している。 この変化を,化学式を使って表せ。 解答C
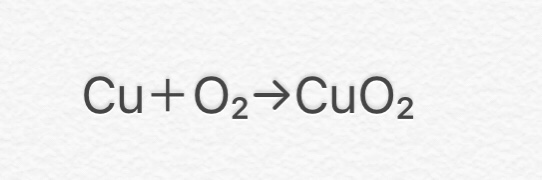



クイズで勉強 中2理科 化学反応式 個別指導塾 現役塾長の話 個別指導塾 現役塾長の話




答えはあるのですが答えになる意味が分かりません 説明お願いします Clear
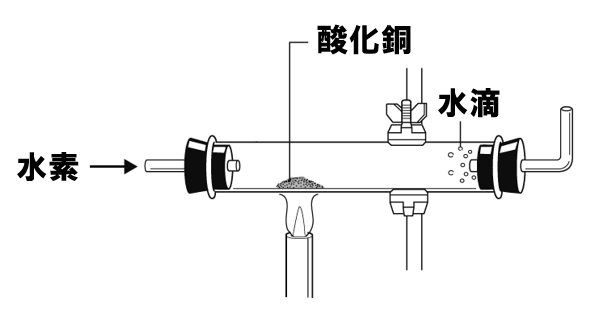
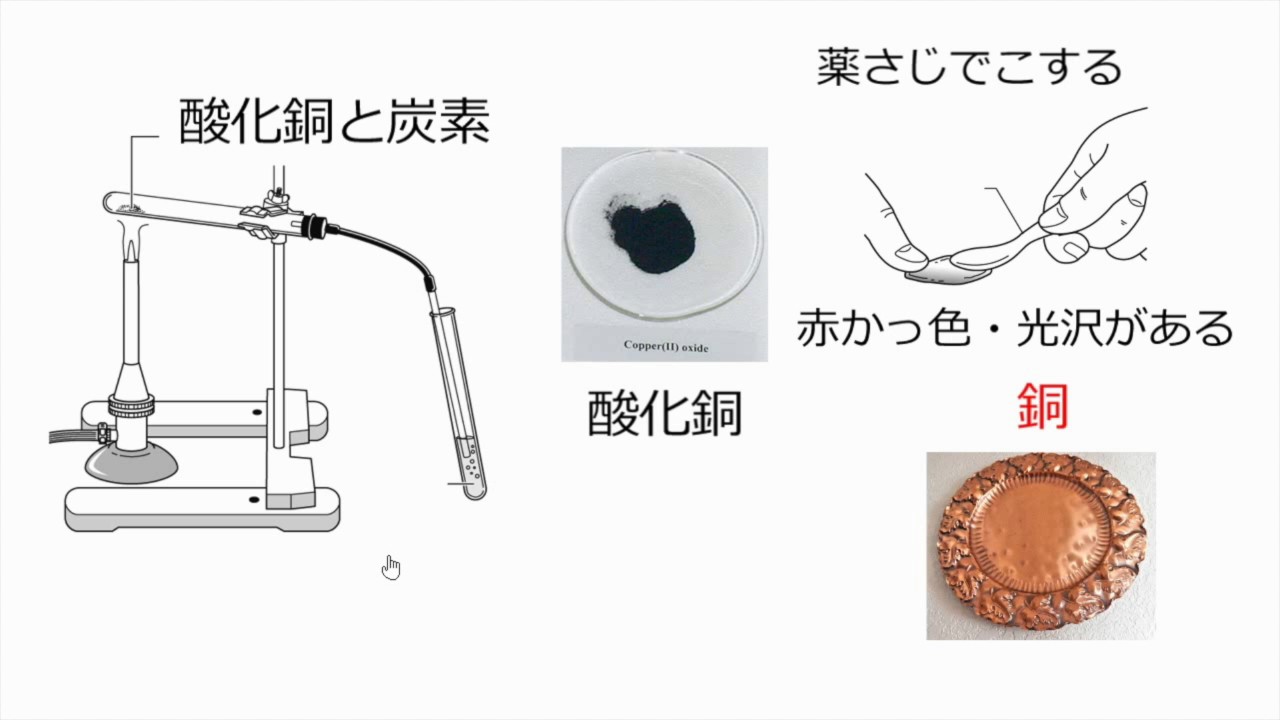
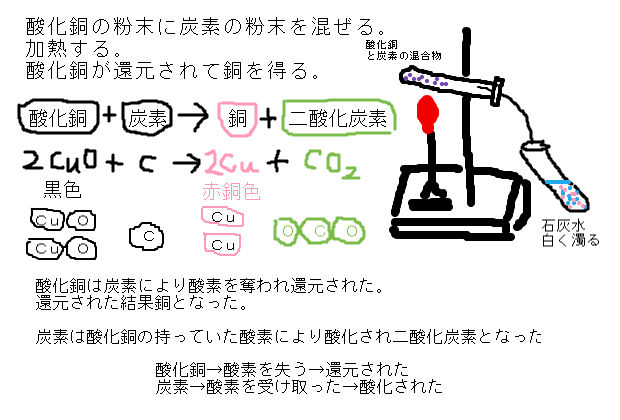
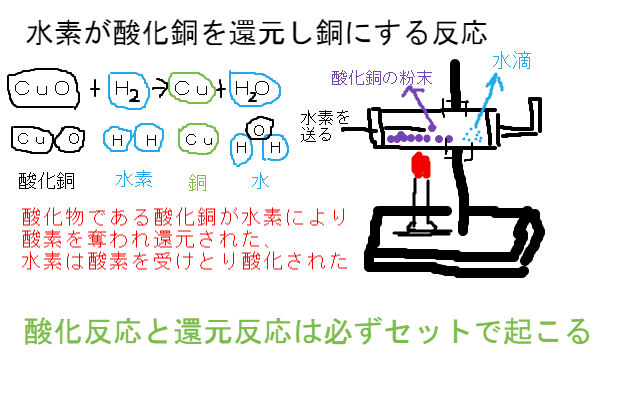
化学反応式 チェックテスト カッコに数字を入れて化学反応式を完成させよ。 ただし数字を入れる必要のないところは空らんにせよ。 水の電気分解 水→水素酸素 2 H2 O → 2 H2 O2 マグネシウムの酸化 マグネシウム酸素→酸化マグネシウム 2銅が酸化すると酸化銅になる User Walkerma on enwikipedia, Public domain, via Wikimedia Commons 銅を空気中の酸素と完全に反応させると,赤かっ色の銅が,黒色に変化しました . では,この黒色の物質は何なのか? また,どのような性質があるのか確認して行き・酸化銅と炭素を混ぜ合わせて熱すると二酸化炭素が発生して銅ができることを見出し、原子・分子モデルを 使って説明する。 ・酸化物から酸素を奪う化学変化を還元といい、還元と酸化は同時に起こることを理解する。 4 実験5 酸化物から酸素を取る化学




中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理




中2理科 酸化銅の還元 映像授業のtry It トライイット
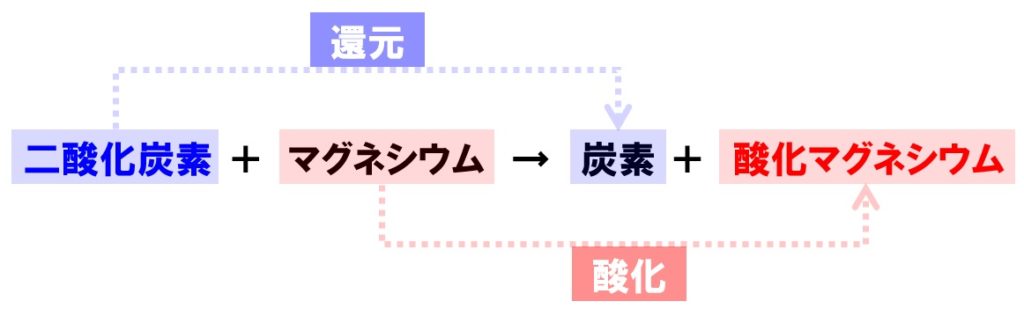
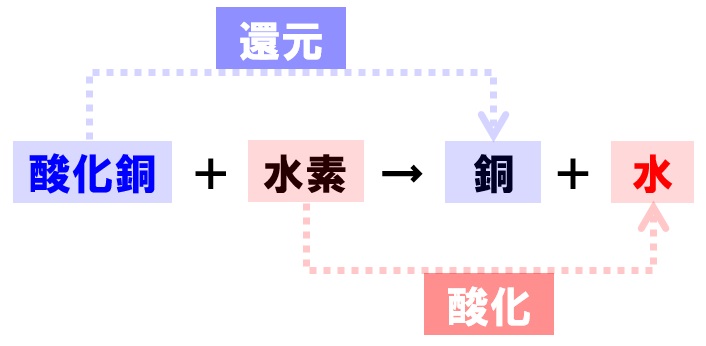
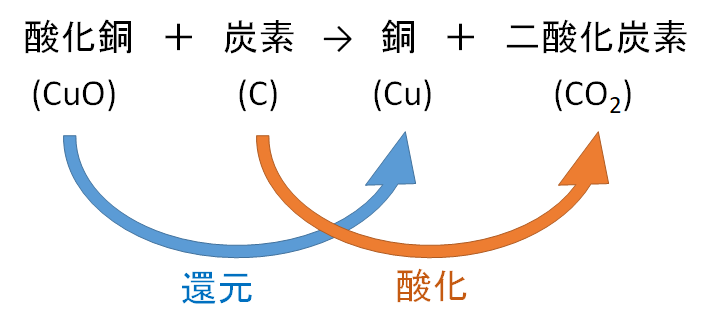
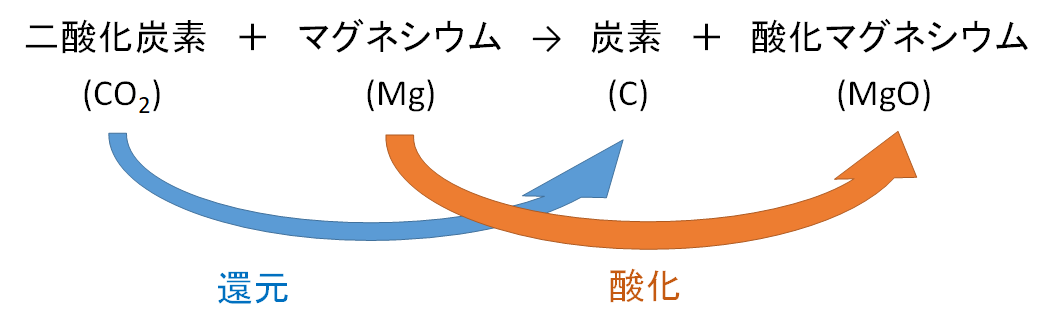
一酸化二炭素(いっさんかにたんそ、dicarbon monoxide)は化学式 C 2 O の無機化合物である。 極めて反応性の高い分子であり、亜酸化炭素の光分解反応によって生成する 。 一酸化炭素、二酸化炭素、亜酸化炭素などのオキソカーボンと密接な関係がある。 一酸化窒素や二酸化窒素との反応を例:水、二酸化炭素、酸化銅 ②混合物 ・2種類以上の物質が混じりあったもの 例:食塩水、空気 4. 化学式 ・原子の記号と数字を用いて物質を表したもの ①分子をつくる物質 ⅰ.単体 ・ h 2 :水素分子 ・ o 2 :酸素分子 ⅱ.化合物 ・ co 2 :二酸化炭素化学変化 化学反応式 酸化銅+炭素→銅+二酸化炭素 2CuO+C→2Cu+CO2 酸化銅+水素→銅+水 CuO+H2→Cu+H2O 二酸化炭素+マグネシウム→炭素+酸化マグネシウム CO2+2Mg→C+2MgO




化学反応式 Ict教材eboard イーボード




中2 理科 中2 10 酸化物から酸素をとり出す Youtube
酸化銅と炭素を混ぜて加熱したところ,銅と二酸化炭素が発生した ことがわかります。 モデルで考えると, 酸化銅 + 炭素 → 銅 + 二酸化炭素 という反応がおこっています。 図3 酸化銅と炭素を よく混ぜ合わせた粉 ゴム ピンチコック 試験管B 試験管A反応式 〔 2h 2 + o 2 → 2h 2 o 〕 炭素 c の燃焼 炭素 c を燃焼する( o 2 と反応させる)と, c 原子と酸素分子 o 2 中の o 原子とが化合して〔 二酸化炭素 co 2 〕ができる。酸化銅と炭素粉末をよく混ぜ合わせて 試験管に入れて加熱した。炭素(c)が酸素 (o)と結びつく力は銅(cu)が酸素と結び つく力よりも強い。そのため,図のよう に,炭素(c)は酸化銅(cuo)の酸素(o)を うばって,二酸化炭素(co 2)になる。酸




Science 還元 働きアリ



実験9 酸化銅の還元 2年理科 化学 Takaの授業記録03
二酸化炭素の中で マグネシウムは燃 えるだろうか。 3 実験を行う。 水上置換で二酸化 炭素を集め,集気び ウムを燃やす。 理由とともに考えさせる。 は高い熱と光を出すから。 展 開 ② ( 2 3 分 ) 4 化学変化を反応式 や,モデルで説明す る。 酸化・還元がこの二酸化炭素の検出反応は、最終的に炭酸カルシウムを沈殿させるものでした。石灰水の成分である水酸化カルシウムCa(OH) 2 ではこの反応を行えますが、同じカルシウムイオンを含む塩化カルシウムCaCl 2 は二酸化炭素と反応を起こしません。それはなぜ化学反応式の例 酸化銀の分解 2Ag 2 O → 4Ag O 2 炭酸水素ナトリウムの分解 2NaHCO 3 → Na 2 CO 3 CO 2 H 2 O 水の分解 2H 2 O → 2H 2 O 2 塩化銅の分解 CuCl 2 → Cu Cl 2 銅の酸化 2Cu O 2 → 2CuO マグネシウムの酸化 2Mg O 2 → 2MgO 炭素の酸化 C O 2 → CO 2 水素の燃焼 2H 2 O 2 → 2H 2 O 鉄と硫黄の化合 Fe S




中2理科 酸化銅の還元 練習編1 映像授業のtry It トライイット



中2理科 酸化銅の還元 酸化も同時に起こる反応 Pikuu
二酸化炭素 (にさんかたんそ、 英 carbon dioxide )は、 化学式 が CO 2 {\displaystyle {\ce {CO2}}} と表される 無機化合物 である 化学式から「シーオーツー」と呼ばれることもある また、 地球温暖化 対策の文脈では、本来は 炭素 そのものを指す「カーボン」と略されることもある(「酸化銅と炭素を加熱し、酸化銅が炭素によって還元されて銅にもどる反応の化学反応式を考えてみよう。 まず、物質名。 酸化銅+炭素→銅+二酸化炭素 化学式で記述する。 CuO+C→Cu+CO2




化学反応式 Ict教材eboard イーボード




中2理科 酸化銅の還元 練習編2 映像授業のtry It トライイット




酸化還元反応 電子のやり取り



中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理



高校入試 理科の 酸化還元 って何 ポイントを整理して苦手克服のコツをすべて伝えます 高校入試徹底対策ガイド




中2理科 酸化銅の還元 映像授業のtry It トライイット




酸化銅の還元 中学生向け



Www Tsukuba Ac Jp Community Students Kagakunome Shyo List 10 Kou 1 Pdf



水酸化銅 を加熱すると 酸化銅 Cuoが生じる という反 Yahoo 知恵袋




都立高校入試理科 酸化銅の還元 対策 坂本良太 Note



中2理科 酸化銅の還元のポイント Examee



中2理科 酸化銅の還元のポイント Examee




酸化銅の還元 中学生向け



化学変化 化合 のまとめ 2年理科 化学 Takaの授業記録03




の所教えてくださいm M ちなみに3番はウを選びました Clear




中2理科 酸化銅の還元 酸化も同時に起こる反応 Pikuu



1




Web教材イラスト図版工房 R C1m 酸化銅の還元の化学反応式のモデル図




中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理



実験9 酸化銅の還元 2年理科 化学 Takaの授業記録03




酸化銅と炭素の混合物を加熱した時に起こる反応を化学反応式で教えてください Clear




T 7k Lihat Cara Penyelesaian Di Qanda




スタディピア 酸化と還元




酸化銅の還元 中学生向け



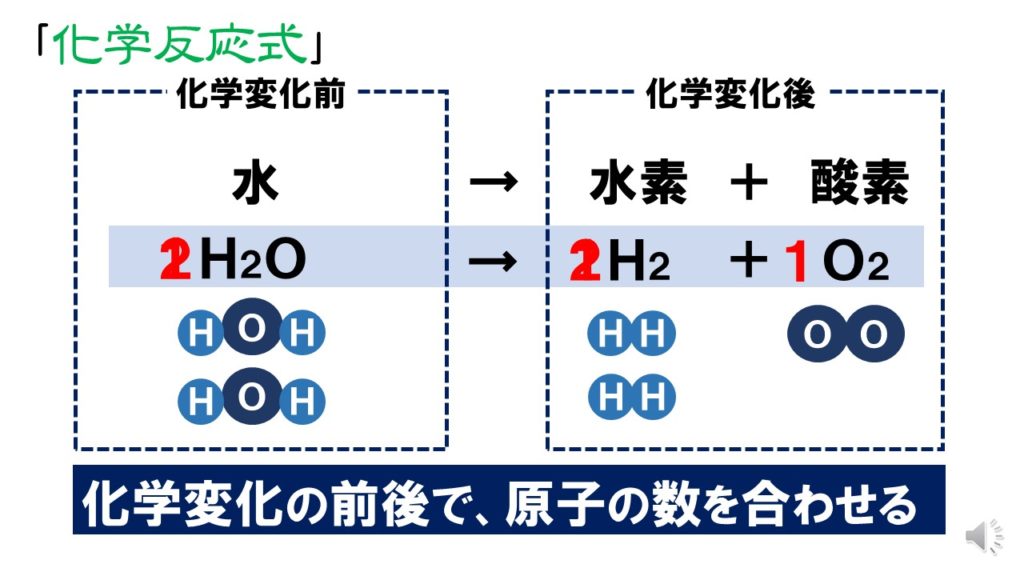
中2理科 化学反応式 のつくり方 Pikuu




なぜ酸化銅を水素によって還元するとき2cuoにならないのですか 炭素ではそうなってい Clear




Science 還元 働きアリ




還元 無料で使える中学学習プリント



中2理科 酸化銅の還元のポイント Examee



Q Tbn And9gcrkjbcruuamxdi Jt1rbyn0uq5inffckuwyilo2vmj Suovgqf Usqp Cau
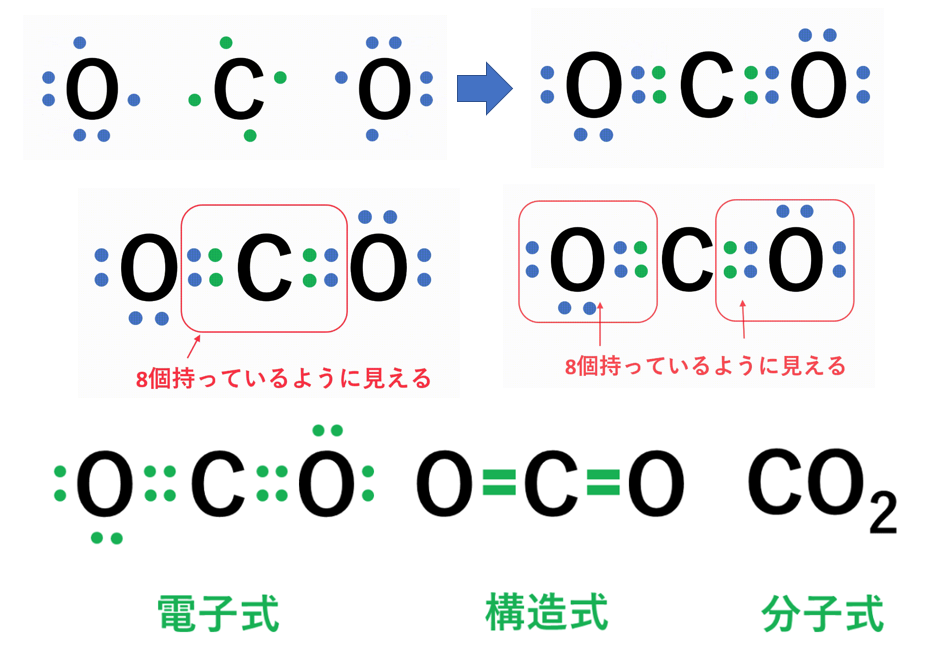



化学反応式




中2理科 酸化銅の還元 映像授業のtry It トライイット
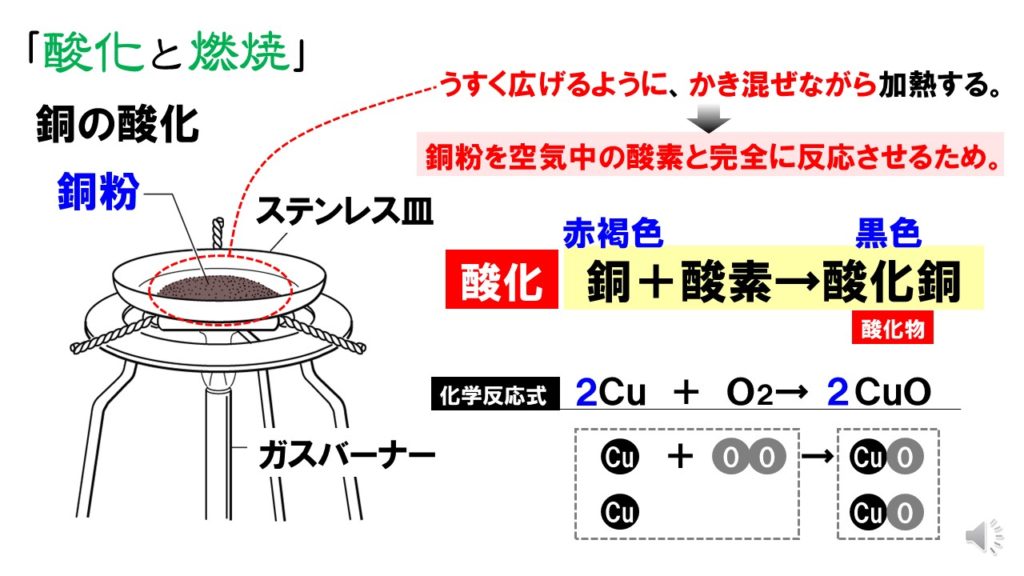



中2理科 酸化と燃焼 銅とマグネシウムの反応 Pikuu




6番から10番まで分かりません 夜遅くに申し訳ないですが 教えてください Clear




この問題の 4 が分かりません 解説お願いします Clear




中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理




中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理
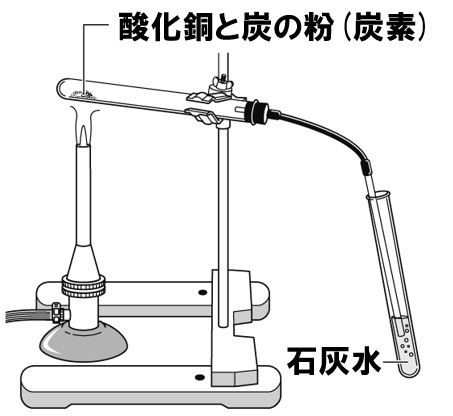



中2理科 酸化銅の還元のポイント Examee
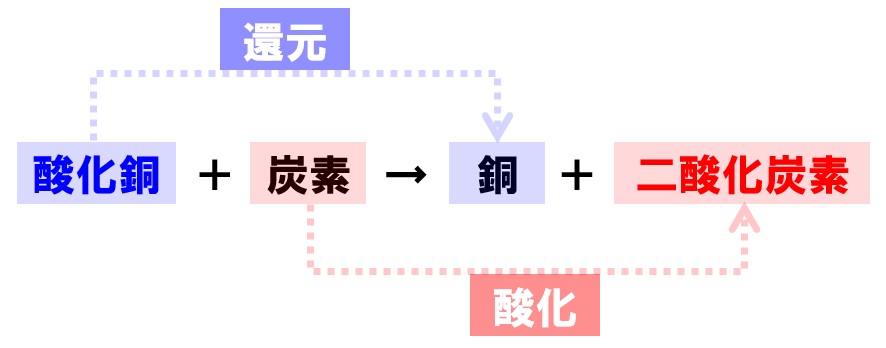



中2理科 酸化銅の還元のポイント Examee



化学変化の計算問題




夕凪亭別館 写真館 10 化学反応式




中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理



主な化学反応式一覧 中学理科で登場する化学反応式のまとめ 教科書をわかりやすく通訳するサイト



酸化銅の炭素による還元 勉強 Youtube スタディチューブ




中学校理科 第1分野 化学変化と原子 分子 Wikibooks




G A Lihat Cara Penyelesaian Di Qanda



Al関連の実践 中学校 理科 振り返りを通して 学びの質 を分析する力を育成する



還元




中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理




中学二年の理科です 酸化還元 Clear




3 40g Descubre Como Resolverlo En Qanda



化学変化の計算問題



中2理科 化学反応式 のつくり方 Pikuu



中2化学 還元 中学理科 ポイントまとめと整理



1



Http Www Adachi Ed Jp Adach6 J Pdf Korona3rdgraderika02kagakuhannoshiki Pdf




Science 還元 働きアリ



中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理




中学理科 酸化銅の還元のグラフ 酸化銅と炭素をよく混ぜ合わせたもの Okwave




中2理科 酸化銅の還元 練習編1 映像授業のtry It トライイット
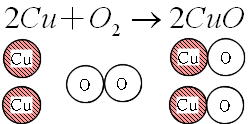



Science 化学変化と質量比 定比例の法則と原子量 分子量 働きアリ



化学式の質問です理科のテキストで酸化銅の化学式が2cu O2 2cuoと解 Yahoo 知恵袋



Www Education Fukaya Saitama Jp Action Common Download Main Upload Id




ここの問い全然わかりません 教えてほしいです Clear




理科 中2 7 化学反応式の作り方 Youtube




T 7k Lihat Cara Penyelesaian Di Qanda



中2化学 還元 中学理科 ポイントまとめと整理




中2 化学 4 1 酸化銅の還元 Youtube



理科2年 化学




無機化学の予備知識




中2理科 酸化銅の還元 酸化も同時に起こる反応 Pikuu



2




酸化銅の還元 中学生向け




中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理



この酸化銅と水素の還元の化学反応式では酸素原子の数が合わないので Yahoo 知恵袋




中2理科 銅 酸素の化学反応式 練習編1 映像授業のtry It トライイット



2 o 問1 次の各化学反応式に係数を入れよ



酸化と還元の問題は速答での得点源 中学数学 理科 寺子屋塾の復習サイト




中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理



Q Tbn And9gctehsdksi7l6bm3okjvjnlufj9n7tjehbedmm0f3j46ram8fxj7 Usqp Cau




スタディピア 酸化と還元



定期テスト対策問題 酸化銅の還元 Examee



理科 なるほどの素




化学反応式の作り方や覚え方 中学生でも簡単に書ける方法 三重の個人契約家庭教師



中2理科 酸化銅の還元のポイント Examee



酸化と還元の問題は速答での得点源 中学数学 理科 寺子屋塾の復習サイト




中2理科 酸化銅の還元 映像授業のtry It トライイット



理科2年 化学




中2理科 酸化銅の還元 練習編2 映像授業のtry It トライイット



Http Www Kure City Jp Miyc Oshirase 2nenrikashikenhaninohennkou Pdf



0 件のコメント:
コメントを投稿